Bệnh viện Ung bướu Hà Nội - Nơi gửi gắm niềm tin và hy vọng
Thứ Hai - Thứ Sáu:
6h00 - 12h00 & 13h00 - 17h00(Thứ 7 khám theo yêu cầu: 7h00 - 12h00)
Email:
bvubhn@hanoi.gov.vnHotline:
1900 8198MỘT SỐ TIẾN BỘ TRONG ĐIỀU TRỊ UNG THƯ PHỔI GIAI ĐOẠN TIẾN XA VÀ DI CĂN
22/06/2024 - 03:37
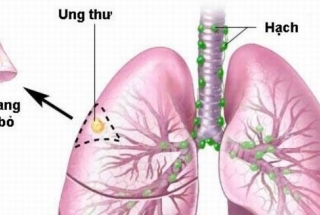
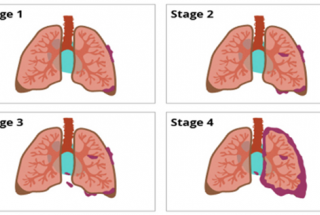
Ung thư phổi (UTP) là bệnh ung thư phổ biến nhất trên toàn cầu và là nguyên nhân gây tử vong do ung thư thường gặp nhất. Tại Việt Nam ghi nhận năm 2018, số ca mắc mới là 23,6 nghìn ca, lớn thứ hai chỉ sau ung thư gan. UTP được chia thành hai nhóm chính là UTP tế bào nhỏ (UTPTBN) và UTP không tế bào nhỏ (UTPKTBN), trong đó UTPKTBN chiếm 80-85%. Do tính chất ác tính của bệnh, đa số các bệnh nhân phát hiện và đến viện khi bệnh đã ở giai đoạn muộn, thể trạng người bệnh yếu, điều này làm cho việc điều trị trở nên khó khăn hơn.3 Gần đây, với sự ra đời và tiến bộ nhanh chóng của y học chính xác (Precision medicine) hay y học cá thể hoá (Personalized medicine), điều trị UTP đã có những bước tiến đáng kể với sự xuất hiện của liệu pháp điều trị nhắm trúng đích và liệu pháp miễn dịch, bên cạnh những phương pháp cơ bản như hoá chất và xạ trị.
1. Liệu pháp điều trị nhắm trúng đích
Trong vòng 30 năm trở lại đây, với sự phát triển của sinh học phân tử, nghiên cứu về hồ sơ di truyền học trong bệnh lý ung thư, đặc biệt là ung thư phổi đã thật sự bùng nổ. Các nhà khoa học đã phát hiện ra các loại đột biến gen quan trọng có ảnh hưởng đến ung thư, còn gọi là ''driver mutation''. Các thuốc đích nhắm vào các đột biến này thông qua các thụ thể trên bề mặt tế bào ung thư, ức chế sự phát triển và thúc đẩy quá trình chết tự nhiên của tế bào u, từ đó làm giảm kích thước và tiêu diệt khối u.
Đối với ung thư phổi, các đột biến được nghiên cứu rộng rãi và đã áp dụng điều trị thành công bao gồm đột biến gen EGFR (Epidermal growth factor receptor - thụ thể của yếu tố tăng trưởng biểu bì) và ALK (Anaplastic lymphoma kinase). Ngoài ra, một số đột biến khác cũng đã được tìm thấy và đã có thuốc điều trị như đột biến gen ROS1, BRAF, KRAS, RET,... hứa hẹn các phương pháp điều trị hiệu quả mới đối với bệnh lý UTP trong tương lai.

1.1 Đột biến gen EGFR
Đây là loại đột biến gen thường gặp nhất ở bệnh nhân UTP, đặc biệt trên quần thể người châu Á, bệnh nhân nữ, không hút thuốc và tế bào ung thư có nguồn gốc từ biểu mô tuyến. Tỷ lệ bệnh nhân UTP châu Á có mang đột biến gen này lên tới 40-50%.
Hiện nay, các thuốc tác động vào đích EGFR có 3 thế hệ đang được sử dụng cho các bệnh nhân UTPKTBN, cụ thể bao gồm:
- Thế hệ 1: thuốc Erlotinib và Gefitinib. Hai thuốc này có hiệu quả điều trị tương đương nhau, giúp kéo dài thời gian sống thêm bệnh không tiến triển khoảng 5-6 tháng so với hoá trị. Ưu điểm của nhóm này là an toàn, ít tác dụng phụ, thường gặp nhất là nổi ban da (với Erlotinib) và tăng men gan (với Gefitinib). Các tác dụng không mong muốn này sẽ được quản lý bởi bác sĩ điều trị bằng các thuốc hỗ trợ khác và hầu hết có thể kiểm soát được.
- Thế hệ 2: Afatinib và Dacomitinib. Các thuốc này đã được chứng minh có hiệu quả không chỉ với những trường hợp mang đột biến gen EGFR thường gặp (như đột biến trên exon 19 - del 19 và exon 21 - L858R), mà còn với những bệnh nhân mang đột biến gen EGFR hiếm gặp - thường kháng với hoá chất (như đột biến trên exon 20: L861Q, G719X và S768I). Tuy nhiên, bên cạnh lợi thế đó, các thuốc thế hệ 2 thường mang lại nhiều độc tính hơn khi sử dụng thuốc như tiêu chảy, viêm ruột, nổi ban da với mức độ độc tính thường nặng hơn so với các thuốc thế hệ 1 và 3.
- Thế hệ 3: Osimertinib. Thuốc Osimertinib không những có khả năng ức chế hoạt động của đột biến gen EGFR, mà còn có thể ức chế đột biến gen T790M - một loại đột biến mắc phải của gen EGFR, thường xuất hiện sau khi bệnh nhân được điều trị với thuốc nhắm trúng đích EGFR thế hệ 1,2 sau khoảng thời gian 9-12 tháng, làm tăng khả năng thất bại với điều trị. Tuy nhiên, các nghiên cứu cho thấy, chỉ khoảng 50-60% các trường hợp người bệnh UTP đã điều trị thuốc nhắm trúng đích thế hệ 1,2 có biểu hiện đột biến này. Ngoài ra, Osimertinib còn được chứng minh có hiệu quả tốt với các tổn thương di căn não - vị trí di căn thường gặp nhất trong UTP.
1.2 Đột biến gen ALK
Trong UTPKTBN, tỷ lệ các bệnh nhân có đột biến ALK là khoảng 3-7%, đa số hay gặp trên các người bệnh trẻ tuổi, phụ nữ, không hút thuốc lá và có thể mô bệnh học khối u là ung thư biểu mô tuyến. Đột biến ALK được phát hiện bằng xét nghiệm hoá mô miễn dịch hoặc lai huỳnh quang tại chỗ (FISH) hay xét nghiệm giải trình tự gen thế hệ mới (NGS - New generation sequencing). Điều trị bằng các thuốc kháng ALK giúp đem lại hiệu quả đáng kể trong việc giúp tăng tỷ lệ đáp ứng của khối u, kéo dài thời gian sống thêm không bệnh, thời gian sống thêm toàn bộ. Ưu điểm của các thuốc này là có ít tác dụng không mong muốn, thông thường là nôn, buồn nôn, mệt mỏi và chủ yếu ở mức độ nhẹ. Các thuốc nhắm trúng đích kháng ALK bao gồm:
- Thế hệ 1: Crizotinib
- Thế hệ 2: Alectinib, Ceritinib, Brigatinib
- Thế hệ 3: Lorlatinib
Các thuốc này đã được nghiên cứu cho thấy hiệu quả rõ rệt trên đối tượng bệnh nhân mắc UTP giai đoạn tiến xa hoặc di căn có đột biến ALK, so với nhóm điều trị hoá chất tiêu chuẩn. Vì vậy, bên cạnh các thuốc nhắm trúng đích EGFR, đây sẽ là giải pháp điều trị đầy hứa hẹn đối với các bệnh nhân UTP.
1.3 Một số đột biến gen khác
Trên thực tế, bên trong các tế bào khối u có thể có rất nhiều loại đột biến khác nhau. Với sự phát triển của y học chính xác và các kỹ thuật hiện đại, ngày nay các nhà khoa học đã nghiên cứu và tìm ra các thuốc nhắm vào đích tác động khác mặc dù tỷ lệ bệnh nhân mang các đột biến này không nhiều. Các thuốc có thể kể đến như:
- Đột biến MET: MET là 1 gen tiền ung thư mã hóa cho thụ thể xuyên màng MET tyrosine kinase. Trong ung thư phổi có 2 hình thức biến đổi chủ yếu của MET đó là protein biểu lộ quá mức và phosphoryl hóa. Tỷ lệ đột biến gen MET khoáng < 5% và thường gặp ở exon 14, liên quan đến các BN lớn tuổi, có tiền sử hút thuốc. Các thuốc ức chế tyrosin kinase đã được sử dụng để nhắm mục tiêu MET trong điều trị UTPKTBN. thuốc Crizotinib là thuốc kháng ALK thế hệ 1, đã được nghiên cứu và cho thấy thuốc có hiệu quả trên nhóm bệnh nhân ung thư phổi giai đoạn tiến xa và di căn có đột biến đột biến MET. Ngoài ra sự khuếch đại gen MET còn gặp ở 4-20% bệnh nhân UTPKTBN có ĐBG EGRF kháng điều trị với các TKIs EGFR. Hướng kết hợp giữa điều trị MET và TKIs EGFR đang được nghiên cứu ở nhóm bênh nhân này.
- Đột biến ROS 1: Gặp khoảng 1-2% trong ung thư phổi. Sự tái sắp xếp gen ROS1 là nguyên nhân gây ung thư phổi. Đặc điểm lâm sàng của nhóm bệnh nhân UTP có ĐBG ROS1 (+) khá tương đồng với nhóm bệnh nhân UTP có ĐBG ALK (+). Crizotinib và Entrectinib, Loratinib là những TKIs đã được chứng minh hiệu quả trong điều trị UTPKTB có ĐBG ROS1 (+). Repotrectinib đang được nghiên cứu và sẽ là 1 triển vọng mới trong tương lai.
- Đột biến BRAF: thuốc Dabrafenib/ Trametinib. Tuy tần suất người bệnh mang đột biến BRAF V600E rất thấp, chỉ khoảng 1-3%, các thuốc mới được nghiên cứu này giúp cải thiện tỷ lệ đáp ứng và thời gian sống thêm bệnh không tiến triển.
- Đột biến KRAS: thuốc Sotorasib đã được Cục quản lý thực phẩm và dược phẩm Hoa Kỳ - FDA cấp phép điều trị với người bệnh mắc ung thư phổi không tế bào nhỏ giai đoạn tiến xa và di căn và có đột biến KRAS G12C và đã thất bại với ít nhất một phác đồ hoá chất. Thuốc giúp kiểm soát bệnh lên tới 80%, trong đó 37% bệnh nhân có đáp ứng với thuốc.9
2. Liệu pháp miễn dịch
Liệu pháp miễn dịch là phương pháp điều trị sử dụng các thuốc tác động nhằm tăng cường hệ thống miễn dịch của cơ thể, giúp chúng nhận dạng, phát triển và chống lại sự tăng sinh của tế bào ung thư trong cơ thể người bệnh. Ngày nay, liệu pháp miễn dịch đã được nghiên cứu nhiều và bước đầu được áp dụng có hiệu quả điều trị bệnh nhân UTP tại nhiều nước trên thế giới. Cụ thể, điều trị miễn dịch với ung thư phổi bao gồm:
2.1 Thuốc ức chế điểm kiểm soát miễn dịch
Điểm kiểm soát miễn dịch (immune checkpoint) là các thụ thể bề mặt, có chức năng điều hoà các tín hiệu tế bào và kìm hãm hoạt động miễn dịch của tế bào lympho T. Trong vi môi trường ung thư, các tế bào ung thư thường tăng cường biểu hiện CTLA-4 ligand, PD-L1 ligand à do đó ức chế hoạt động của tế bào T.
PD-1 (programmed cell death receptor 1) là thụ thể ức chế miễn dịch được xác định sau CTLA-4. Thụ thể này có 2 ligand là PD-L1 và PD-L2. PD-1 là thụ thể điều hoà âm tính, gắn trên bề mặt tế bào lympho T đã hoạt hoá
PD-L1 là một protein xuyên màng typ 1 có mặt trên các tế bào u thúc đẩy quá trình điều hoà và tự dung nạp của hệ miễn dịch loại bỏ tế bào u thông qua ức chế hoạt động gây viêm của tế bào T bằng cách gắn với thụ thể tế bào lympho T điều hoà – PD-1
Khi PD-L1,2 gắn với PD-1 sẽ truyền tín hiệu ức chế miễn dịch cho tế bào T, dẫn đến trạng thái “bất hoạt” của tế bào T à ức chế hoạt động tế bào T. PD-1 chủ yếu kiểm soát hoạt động của tế bào T hoạt hoá ở mô ngoại biên. Bên cạnh đó, con đường PD-1/PD-L1 cũng được cho là có vai trò trong việc điều khiển quá trình xâm nhập của tế bào T vào trong khối u, do đó ngăn sự tiếp xúc trực tiếp của tế bào T hoạt hoá và tế bào ung thư . Do đó, kháng thể kháng PD-1 hoặc kháng PD-L1 lần lượt sẽ tương tác với PD-1 hoặc PD-L1, giúp tái hoạt hoá tế bào T bị “bất hoạt” hay giải phóng ức chế.

Có nhiều thuốc miễn dịch đã được chấp thuận điều trị UTP. Một vài trong số các thuốc này hoạt động dựa trên cơ chế ngăn cản sự liên kết giữa protein PD-L1 và thụ thể PD-1. Việc ngăn cản mối tương tác này giúp cho hệ thống miễn dịch của cơ thể nhận ra, bắt đầu tấn công và tiêu diệt các tế bào ung thư. Các thuốc này gồm Pembrolizumab, Atezolizumab, Nivolumab ...
Một chốt kiểm soát miễn dịch khác cũng được nghiên cứu nhiều, đó là CTLA4. Khi điểm này bị khoá, cơ thể người bệnh có thể tăng sản xuất hàng loạt các tế bào miễn dịch để sẵn sàng chống lại các tế bào ung thư. Các thuốc trong nhóm này có thể kể đến là Ipilimumab, Tremerimumab.
Tác dụng không mong muốn của thuốc miễn dịch tương đối ít, bao gồm mệt mỏi, buồn nôn, ngứa, phát ban,... và đa số ở mức độ nhẹ. Tuy nhiên, nó có thể gây ra các độc tính nguy hiểm liên quan đến đáp ứng miễn dịch quá mức ở một số cơ quan, biểu hiện: viêm ruột, suy giáp hay cường giáp,...
2.2 Vaccin chống ung thư
Các tế bào ung thư có chứa các chất gọi là kháng nguyên, đóng vai trò là tác nhân lạ đối với cơ thể. Các kháng nguyên này vốn không có hoặc có rất ít trên bề mặt các tế bào bình thường. Liệu pháp vaccin sẽ giúp hệ thống miễn dịch nhận biết và tiêu diệt tế bào ung thư dễ dàng hơn. Tuy còn đang trong giai đoạn thử nghiệm nghiên cứu lâm sàng, liệu pháp này hứa hẹn sẽ là biện pháp điều trị mới và hiệu quả cao trong điều trị bệnh lý ung thư nói chung và UTP nói riêng.
2.3 Liệu pháp CAR-T

Trong phương pháp này, các tế bào lympho T (một trong những loại tế bào miễn dịch của cơ thể) được lấy ra khỏi cơ thể người bệnh, sau đó được xử lý trong phòng thí nghiệm để làm tăng khả năng nhận diện đối với tế bào ung thư. Sau đó, các tế bào lympho T đã được xử lý này được đưa trở lại vào cơ thể người bệnh, giúp chống lại khối u. Đây cũng là phương pháp điều trị miễn dịch mới, đang được nghiên cứu nhiều trong các thử nghiệm lâm sàng và hiện tại chưa được chấp thuận để điều trị bệnh UTP. Trong tương lai, đây cũng là liệu pháp điều trị miễn dịch đầy hứa hẹn.
Tóm lại, với sự tiến bộ vượt bậc của y học và khoa học công nghệ, việc điều trị bệnh lý ung thư phổi giai đoạn tiến xa và di căn đã có nhiều lựa chọn mới với kết quả điều trị cải thiện đáng kể so với các phương pháp điều trị căn bản, đem lại tác dụng kéo dài thời gian sống thêm và nâng cao chất lượng cuộc sống cho người bệnh.
Biên soạn: BS. Phùng Ngọc Nam – Khoa Nội Tổng hợp Theo yêu cầu
Kiểm duyệt: BSCKII. Lê Thị Lệ Quyên – Trưởng khoa Nội Tổng hợp Theo yêu cầu
Thiết kế: ThS. Nguyễn Hà My - Phòng QLCL-CTXH
Tài liệu tham khảo: